Die Entwicklung von Medikamenten ist mit hohen Risiken verbunden und zeitaufwändig. Das Warten auf potenzielle neue Behandlungsmethoden ist für Patienten, insbesondere für Patienten mit seltenen oder schwer behandelbaren Krankheiten, hart. Und wenn der Markt klein ist, können die Kosten für das zugelassene Medikament hoch sein. Die Umwidmung und Neupositionierung bestehender Medikamente (auch als Reprofilierung bezeichnet) kann den Prozess beschleunigen und die erforderlichen finanziellen Investitionen im Vergleich zu neuen Medikamenten senken. So wird sichergestellt, dass Patienten schneller und zu günstigeren Kosten Zugang zu Behandlungen erhalten.[1, 2]
Es gibt vier Hauptgruppen von umgewidmeten Medikamenten: Medikamente, die unter bestehenden oder abgelaufenen Patenten vermarktet werden, Medikamente, deren Zulassung im klinischen oder regulatorischen Stadium eingestellt wurde, Stereoisomere oder Metaboliten bestehender Medikamente oder Kandidaten, an denen geringfügige Änderungen vorgenommen wurden. Es ist wichtig, sich daran zu erinnern, dass das Scheitern von Medikamenten in klinischen Studien nicht nur auf Wirksamkeits- oder Sicherheitsprobleme zurückzuführen ist – es kann auch daran liegen, dass ein Unternehmen seine Ausrichtung ändert, Probleme mit der Formulierung hat oder es Probleme mit kommerziellen Interessen oder schlechter strategischer Planung gab.[3]
Die Vorteile der Umwidmung und Neupositionierung von Arzneimitteln
Obwohl die beiden Begriffe häufig synonym verwendet werden, kann sich die Neuverwendung von Arzneimitteln darauf beziehen, dass ein zugelassenes Arzneimittel für eine andere Indikation verwendet wird. Die Neupositionierung von Arzneimitteln kann sich darauf beziehen, die Entwicklung eines ins Stocken geratenen Arzneimittels wiederaufzunehmen, um die Zulassung für eine neue Indikation zu erhalten.[1]
Die Hauptvorteile der Umwidmung oder Neupositionierung von Medikamenten liegen in den Kosten und der Zeit. Der Zeitrahmen für die Entwicklung eines umgewidmeten Medikaments beträgt in der Regel ein bis drei Jahre, verglichen mit durchschnittlich 12 Jahren für ein neuartiges Medikament.[4]
Ein Unternehmen, das ein Medikament entwickelt, dessen Entwicklung ins Stocken geraten ist oder das bereits für eine andere Indikation auf den Markt gekommen ist, kann durch die Möglichkeit, die vorhandenen präklinischen und/oder klinischen Daten zur Sicherheit, Toxizität und Pharmakokinetik/Pharmakodynamik „wiederzuverwenden“, sowohl Geld als auch Zeit sparen. Außerdem kann das Unternehmen so das Geld zurückgewinnen, das in ein Medikament investiert wurde, das sonst möglicherweise fehlgeschlagen wäre. Das vorhandene Wissen verringert außerdem das Risiko eines Misserfolgs.
Medikamente, deren Entwicklung fehlgeschlagen ist oder scheitert, für die aber noch ein gewisser Patentschutz besteht, können vom Originalhersteller oder einem Lizenznehmer für eine andere Indikation neu positioniert werden. Durch die Neuausrichtung können Unternehmen auch die Lebensdauer ihrer eigenen vermarkteten Medikamente verlängern, deren Patentschutz bald ausläuft, da sie Schutz für die neue Indikation erhalten können. Die Neuausrichtung und Neupositionierung von Medikamenten kann auch für Unternehmen, die Medikamente für seltene Krankheiten entwickeln, von Nutzen sein, da sie die Zusammenarbeit und den Austausch von Daten und Ressourcen fördert.[3, 5]
Die Schritte zur Entwicklung und Zulassung eines zweckentfremdeten Arzneimittels können Folgendes umfassen:
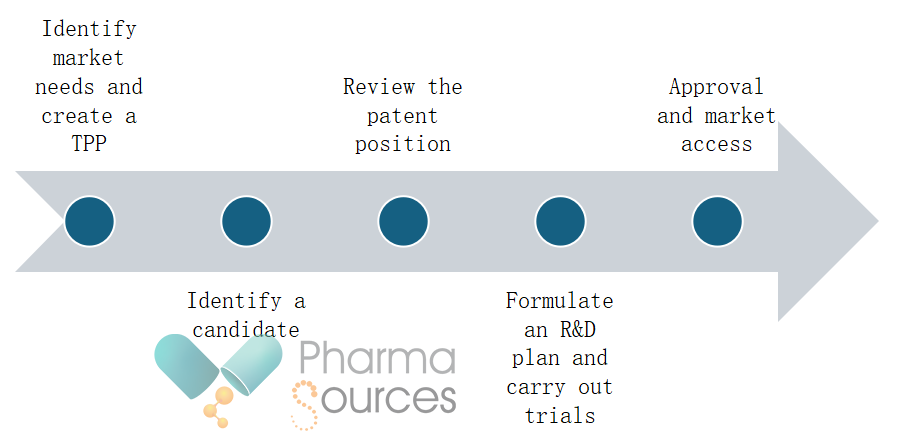
Identifizieren Sie die Marktbedürfnisse und erstellen Sie ein Zielproduktprofil
Für ein Unternehmen, das ein Medikament einer neuen Anwendung zuführen möchte, aber keinen bestehenden Kandidaten im Auge hat, besteht der erste Schritt darin, das Marktumfeld zu bewerten, um zu sehen, ob ein Bedarf der Patienten an einem neuen Medikament besteht und ob das Unternehmen die Investition in die Medikamentenentwicklung wieder hereinholen kann. Dies wird durch die Entwicklung eines Zielproduktprofils (TPP) unterstützt. Das TPP beschreibt die gewünschten Eigenschaften eines in der Entwicklung befindlichen Medikaments für eine bestimmte Erkrankung. Es dient dem Unternehmen als Leitfaden für alle beteiligten Teams während der gesamten Medikamentenentwicklung. [2, 6, 7]
Zu den von einer TPP abgedeckten Bereichen, deren Überprüfung auch dann sinnvoll ist, wenn ein Unternehmen einen bestimmten Kandidaten im Auge hat, gehören:[2, 7, 8]
●Anzeige
○Erste Zielanzeige
○Potenzielle zukünftige Indikationen
●Bevölkerung
○Anfänglicher Zielmarkt – wirtschaftliche Prioritäten oder Bereiche mit dem größten ungedeckten Bedarf
○Durchführbarkeitsstudie
○Bedarf an einer Begleitdiagnostik zur Identifizierung von Subpopulationen
●Zielgerichtete Therapie/Pharmakokinetik
●Sicherheit, Verträglichkeit und Wirksamkeit
○Studienziele
○Vorteile im Vergleich zu aktuellen/zukünftigen Wettbewerbern oder zum Behandlungsstandard
●Wechselwirkungen zwischen Arzneimitteln
●Stabilität
○Anforderungen an die Lagerung
○Kann von Zielmärkten abhängen
● Verabreichungsweg/Formulierung
○Aktuelle Formulierung/Potenzial für Neuformulierung
○Welche Verabreichungsart werden die Patienten bevorzugen?
○Wird ein Liefergerät benötigt und ist es bereits verfügbar?
●Dosierungshäufigkeit
○Vergleich mit dem Standard der Versorgung
●Kosten
○Zielkosten pro Dosis, basierend auf einer Wettbewerbsanalyse
●Zeit bis zur Verfügbarkeit
○ Erforderliche Zeit für klinische Studien und Zulassungsprozesse
○ Erforderlicher Zeitaufwand für Gesundheitstechnologiebewertungen (HTAs)
Einen Kandidaten identifizieren
Ein Unternehmen hat möglicherweise ein Arzneimittel im Auge, das einer anderen Verwendung zugeführt werden soll, und stützt seine neue Indikation beispielsweise auf die Erkenntnis, dass es sich bei einem früheren Entwicklungsprozess um eine Nebenwirkung handelte.

Für ein Unternehmen, das ein Medikament für ein bestimmtes Ziel oder eine bestimmte Indikation sucht, können die Ansätze auf Ziel-, Struktur-, Signatur-, Pfad-, Netzwerk-, Wissens- oder klinischen Daten basieren. Zu den spezifischen Ansätzen gehören:[13-17]
● Mendelsche Randomisierung zur Ermittlung von Beziehungen zwischen Phänotypen und genetisch vorhergesagten Arzneimittelwirkungen
● Umfangreiche Multi-Omics-Daten, um die Krankheitsätiologie besser zu verstehen und neue Wirkstoffziele zu identifizieren
● Maschinelles Lernen zur Identifizierung von Krankheitssubtypen und Arzneimittelzielen oder zur Verknüpfung von Pathologie und molekularen Mechanismen
●Generative KI oder Integration menschlicher Genexpression, Arzneimittelstörungen und klinischer Daten zur Identifizierung von Kandidaten
Überprüfen Sie die Patentposition
Ein Unternehmen, das ein Medikament einer anderen Anwendung zuführen oder neu positionieren möchte, muss sich über die bestehende Patentlage im Klaren sein, einschließlich der Patente für die ursprüngliche Verbindung sowie für Formulierungen, Dosierungsschemata oder spezifische Anwendungen. Wenn das Medikament noch patentgeschützt ist, muss das Unternehmen den Patentinhaber kontaktieren und fragen, ob dieser an einer Zusammenarbeit oder einer Lizenzierung des Medikaments interessiert ist. Wenn das Medikament nicht mehr patentgeschützt ist, besteht eine größere Handlungsfreiheit.[4]
Alle Medikamente, auch umfunktionierte und neu positionierte Medikamente, benötigen ein gewisses Maß an Patentschutz, damit das umfunktionierende Unternehmen seine Kosten wieder hereinholen kann, bevor es mit der Konkurrenz konfrontiert wird. Zu den neuen Patentarten könnten gehören: [4, 18]
●Therapeutische Indikation
●Formulierung
●Dosierungsschema
● Liefersystem
● Kombination von Medikamenten
●Medikament/Gerät-Kombination
Formulieren Sie einen F&E-Plan und führen Sie Versuche durch
Um ein umgewidmetes Medikament erfolgreich zu entwickeln, müssen Unternehmen mit Klinikern und einem multidisziplinären Team aus internen und externen Experten zusammenarbeiten, um den Entwicklungsprozess zu unterstützen. Umgewidmete Medikamente müssen noch über ausreichende präklinische Daten verfügen, klinische Tests durchlaufen und strenge regulatorische Standards für ihre neue Indikation erfüllen. Während vorhandene Daten von Menschen und anderen Personen die Sicherheit und Toxizität belegen, sind weitere klinische Studien erforderlich, um die Wirksamkeit in der Zielpatientengruppe zu bestätigen, bevor sie zur Zulassung eingereicht werden können.[8]Darüber hinaus ist die Zusammenarbeit mit Patienten und Patientenvertretungen wichtig, um ihre Anforderungen an eine Behandlung zu verstehen und Teilnehmer für klinische Studien zu gewinnen.[4]
Zulassung und Marktzugang
Eine enge Zusammenarbeit mit den Zulassungsbehörden und den Gremien für die Bewertung von Gesundheitstechnologien (HTA) unterstützt einen effizienten Prozess hin zu Zulassung, Markteinführung und Kostenerstattung. Die Zulassungsbehörden können beraten, welche klinischen Studien erforderlich sind, und vorschlagen, welcher Weg zur Zulassung (einschließlich beschleunigter Verfahren) für ein bestimmtes Medikament und eine bestimmte Indikation am besten geeignet ist.[4]
Zusammenfassend
Die Umwidmung und Neupositionierung von Medikamenten bietet einen kostengünstigen und effizienten Weg zur Marktreife, der es Patienten ermöglicht, schneller Zugang zu Medikamenten zu erhalten. Unternehmen müssen sicherstellen, dass sie die richtigen Daten sammeln, um einen reibungslosen Ablauf zu gewährleisten. Dies kann durch die Zusammenarbeit mit Patienten, anderen Unternehmen, Aufsichtsbehörden und Gremien zur Bewertung von Gesundheitstechnologien unterstützt werden.
Verweise
1. Bakker, A., Ein scheinbar kleines semantisches Problem ist ein großes Hindernis für die Entwicklung von Behandlungen für seltene Krankheiten. STAT, 2023. Verfügbar unter: https://www.statnews.com/2023/06/27/drug-repurposing-repositioning-rare-diseases/.
2. Griffiths, A., et al., Target Product Profiles in Pharmaceutical Development KPMG. 2023. Verfügbar unter: https://assets.kpmg.com/content/dam/kpmg/uk/pdf/2023/01/target-product-profiles-in-pharmaceutical-development.pdf.
3. Elvidge, S., Getting The Drug Repositioning Genie Out Of The Bottle. Life Science Leader, 2010. Verfügbar unter: https://www.lifescienceleader.com/doc/getting-the-drug-repositioning-genie-out-of-the-bottle-0001.
4. Pisani, J. et al., Repurposing medicines: the opportunity and the challenge. 2021. Verfügbar unter: https://www.lifearc.org/wp-content/uploads/2024/03/RD-Drug-repurposing-report.pdf.
5. Taylor, M., M. Salova und A. Schroeder, Drug Repurposing: Potential to Expand Rare Disease Treatment. Avalere: Insights & Analysis, 19. Februar 2024. Verfügbar unter: https://avalere.com/insights/drug-repurposing-potential-to-expand-rare-disease-treatment.
6. Redakteur. Target-Produktprofile. Weltgesundheitsorganisation. 9. Juli 2024. Verfügbar unter: https://www.who.int/observatories/global-observatory-on-health-research-and-development/analyses-and-syntheses/target-product-profile/who-target-product-profiles.
7. Mitarbeiterautor. Umwidmung eines Medikaments: wichtige Überlegungen. UCL Therapeutic Innovation Networks – UCL – University College London. 9. Juli 2024. Verfügbar unter: https://www.ucl.ac.uk/ion/translation-enterprise/tailored-support-translational-researchers/re-purposing-drug/repurposing-drug.
8. Redakteur. Repurposing Medicines Toolkit – Anleitung zur Navigation durch den Prozess. LifeArc/Medical Research Council. 11. Juli 2024. Verfügbar unter: https://www.repurposingmedicines.org.uk.
9. Runder Tisch zur Umsetzung genombasierter Forschung für die Gesundheit, Board on Health Sciences Policy und Institute of Medicine, in Drug Repurposing and Repositioning: Workshop-Zusammenfassung. 2014: Washington (DC).
10. Ghofrani, HA, IH Osterloh und F. Grimminger, Sildenafil: von Angina pectoris über erektile Dysfunktion bis hin zu pulmonaler Hypertonie und darüber hinaus. Nat Rev Drug Discov, 2006. 5(8): p. 689-702.
11. Gohel, D., et al., Sildenafil als Wirkstoffkandidat für die Alzheimer-Krankheit: Beobachtung realer Patientendaten und mechanistische Beobachtungen an patienteninduzierten pluripotenten, aus Stammzellen gewonnenen Neuronen. J Alzheimers Dis, 2024. 98(2): S. 643-657.
12. Dorset Medicines Advisory Group, SHARED CARE GUIDELINE FÜR SILDENAFIL ZUR BEHANDLUNG DES SEKUNDÄREN RAYNAUD-PHÄNOMENS IM ZUSAMMENHANG MIT SYSTEMISCHER SKLEROSE NHA. 2017. Verfügbar unter: https://nhsdorset.nhs.uk/Downloads/aboutus/medicines-management/Shared%20Care%20Guidelines/Sildenafil%20Shared%20Care%20Documented%20July%2017.pdf.
13. Wang, L. et al., Die Landschaft der Methodik bei der Neuverwendung von Arzneimitteln unter Verwendung menschlicher Genomdaten: eine systematische Überprüfung. Brief Bioinform, 2024. 25(2).
14. Sperry, M. und DE Ingber, Drug Repurposing Strategies, Challenges and Successes. 4. März 2024. Verfügbar unter: https://www.technologynetworks.com/drug-discovery/articles/drug-repurposing-strategies-challenges-and-successes-384263#D3.
15. Rodriguez, S. et al., Maschinelles Lernen identifiziert Kandidaten für die Neuverwendung von Medikamenten bei Alzheimer-Krankheit. Nat Commun, 2021. 12(1): S. 1033.
16. Yan, C., et al., Nutzung generativer KI zur Priorisierung von Kandidaten für die Arzneimittelneuverwendung bei Alzheimer mit klinischer Validierung in der Praxis. NPJ Digit Med, 2024. 7(1): S. 46.
17. Wu, P., et al., Integration von Genexpression und klinischen Daten zur Identifizierung von Kandidaten für die Neuverwendung von Arzneimitteln gegen Hyperlipidämie und Bluthochdruck. Nat Commun, 2022. 13(1): S. 46.
18. Conour, J., Warum sich die Investition in Behandlungspatente für wiederverwendete Arzneimittel lohnt. JD Supra: News & Insights, 5. Oktober 2020. Verfügbar unter: https://www.jdsupra.com/legalnews/why-method-of-treatment-patents-for-92813/.

